Miti comuni: pulizia con disinfettanti in ambienti controllati
Punti chiave:
I dati di monitoraggio ambientale (EM) non costituiscono sempre un indicatore affidabile del rischio di contaminazione, poiché rappresentano solo un'istantanea nel tempo e potrebbero non avere alcun nesso con l'effettiva esposizione del prodotto o con le prestazioni del processo asettico.
I residui di disinfettanti non sono di per sé rischiosi per la qualità del prodotto e la convinzione che i residui ospitino microrganismi vitali non ha fondamento scientifico; la gestione dei residui deve seguire un approccio basato sul rischio.
Spruzzare disinfettanti non garantisce automaticamente risultati migliori rispetto a strofinare un panno o pulire con il mocio, poiché l'efficacia dipende dalla copertura completa della superficie e l'azione meccanica dello strofinamento può migliorare la rimozione dei microbi.
L'uso periodico di disinfettanti e sporicidi è fondamentale per mantenere il controllo della camera bianca, ma le ipotesi sui limiti di tali prodotti, come lo sviluppo di resistenza o l'interferenza dei residui, devono essere valutate criticamente.
Le strategie di applicazione dei disinfettanti devono essere adattate a fattori specifici della struttura, tra cui tipi di superficie, accessibilità dell'area e tendenze dei pregressi dati di EM, anziché basarsi su pratiche generalizzate oppure obsolete.
Parlare di microbiologia farmaceutica e di camere bianche porta inevitabilmente a confrontarsi con una serie di falsi "miti" radicati e persino avallati dagli enti regolatori.
La microbiologia è un argomento in cui dominano falsi miti e idee sbagliate, dalla “regola dei 5 secondi” per mangiare il cibo caduto a terra alle tradizioni popolari, tramandate di generazione in generazione, che consigliano di digiunare quando si ha il raffreddore e di mangiare quando si ha la febbre. Parlare di microbiologia farmaceutica e di camere bianche porta inevitabilmente a confrontarsi con una serie di falsi "miti" radicati e persino avallati dagli enti regolatori. Ad esempio, alcune autorità insistono ancora sulla rotazione dei disinfettanti per prevenire lo sviluppo di ceppi batterici resistenti. Gli autori si propongono di applicare la logica e rigorosi principi scientifici per sfatare alcuni falsi miti che interessano la microbiologia, in particolare la pulizia con disinfettanti degli ambienti controllati.
Si riportano di seguito alcune delle credenze, pratiche e politiche discutibili in cui ci siamo imbattuti:
MITO: i dati del monitoraggio ambientale (EM) costituiscono un affidabile indicatore di rischio rispetto alla qualità del prodotto.
REALTÀ: i dati del monitoraggio ambientale relativi a microrganismi vitali rappresentano generalmente un’istantanea nel tempo e riflettono una condizione transitoria che potrebbe persistere o meno. Un singolo dato (ad esempio, un campione di superficie) non può necessariamente essere considerato rappresentativo al di fuori dei parametri specifici del campione stesso. Gli autori hanno osservato simulazioni di processi asettici contaminati (test di riempimento con terreno di coltura) in cui i dati di EM associati risultavano completamente puliti (0 CFU). Al contrario, hanno osservato risultati conformi in un test di riempimento con terreno di coltura, mentre i dati di EM associati mostravano contaminazioni anormalmente elevate e numerose superamenti dei livelli di allerta e azione. L'interpretazione dei dati di EM delle camere bianche è una pratica molto delicata, che può essere svolta al meglio solo da operatori adeguatamente addestrati, formati ed esperti.
MITO: i residui di disinfettanti essiccati sulle superfici rappresentano un rischio intrinseco per la qualità del prodotto farmaceutico.
REALTÀ: qualsiasi residuo presente su una superficie, se nelle condizioni appropriate, può rappresentare un rischio per la qualità. La teoria secondo cui i residui di disinfettanti possano ospitare microrganismi vitali è un’ipotesi non dimostrata e risulta piuttosto inverosimile, se si considerano le esigenze metaboliche dei microrganismi vitali. Un approccio che affronti il problema dei residui di disinfettante o di qualsiasi altro prodotto nelle camere bianche sulla base del rischio rappresentano e dei principi della scienza è l’unica via consigliabile.
MITO: spruzzare disinfettanti sulle superfici consente di ottenere una copertura maggiore, e quindi un'efficacia maggiore, rispetto a strofinare un panno o pulire con il mocio. REALTÀ: la tecnica è importante! I disinfettanti chimici liquidi agiscono per contatto diretto con le membrane cellulari. La nebulizzazione può essere efficace se si assicura una copertura contigua. Anche l'azione meccanica di strofinare un panno o pulire con il mocio presenta ulteriori vantaggi. Confrontare i due metodi non è un esercizio semplice o immediato. Le aziende devono prendere in considerazione molti fattori per stabilire qual è la modalità di applicazione ottimale per i loro processi e le loro strutture, tra cui: materiali e complessità delle superfici, dimensioni e accessibilità delle aree, pregressi dati di EM. Una valutazione formale dei rischi può essere utile per stabilire l'approccio migliore.
MITO: il recupero di muffa da una superficie durante l’EM richiede un'azione correttiva che consiste nell'impiego di uno sporicida sulla superficie interessata.
REALTÀ: come accennato in precedenza, i risultati dell’EM rappresentano un'istantanea nel tempo e solitamente riflettono condizioni transitorie. Considerato l’intervallo intercorrente tra il prelievo del campione e la comunicazione dei risultati (in genere 3-5 giorni), è possibile che nella zona si siano verificate numerose attività tali da rendere irragionevole intervenire come se le condizioni fossero rimaste immutate. Spesso la superficie interessata è già stata trattata con un detergente germicida con efficacia fungicida. Prevenire è meglio che curare: un'indagine approfondita sulla fonte della muffa e interventi volti a prevenirne la ricomparsa rappresentano l’approccio migliore e scientificamente più valido.
Mito: Melius abondare quam deficere
Nel corso di numerose sopralluoghi presso aziende operanti nel settore biofarmaceutico e della produzione di dispositivi medici, gli autori hanno osservato l'impiego di regimi complessi per la disinfezione delle superfici delle camere bianche, che prevedono l'impiego di 3 o più varietà di disinfettanti e molteplici tipi di sporicidi. Ad esempio, diverse aziende che hanno visitato di recente nell’America meridionale implementano schemi complessi di questo tipo. Questi approcci complessi rendono la disinfezione delle camere bianche gravosa per gli operatori addetti a tale compito, senza aggiungere alcun vantaggio in termini di controllo della carica batterica. Il fatto è che l'uso sistematico di un singolo detergente germicida ad ampio spettro, associato all'uso periodico e mirato di uno sporicida, rappresenta un programma assolutamente efficace per ottenere un controllo adeguato della carica microbica nella stragrande maggioranza degli ambienti delle camere bianche1.
D: Se uno sporicida è in grado di eliminare tutti i microrganismi, perché non usarlo sempre?
R: L'inattivazione chimica delle endospore batteriche richiede formulazioni piuttosto aggressive, come ipoclorito di sodio o miscele di perossido di idrogeno e acido peracetico/acido acetico (PAA). L'uso troppo frequente di uno sporicida a base di ossidante può causare problemi di corrosione nella camera bianca, oltre a problematiche legate all’esposizione per la salute, la sicurezza e l’ambiente. Pertanto, gli sporicidi devono essere usati con cautela, basando la frequenza sul rischio e sui dati dei pregressi EM relativi al recupero di batteri che formano endospore.
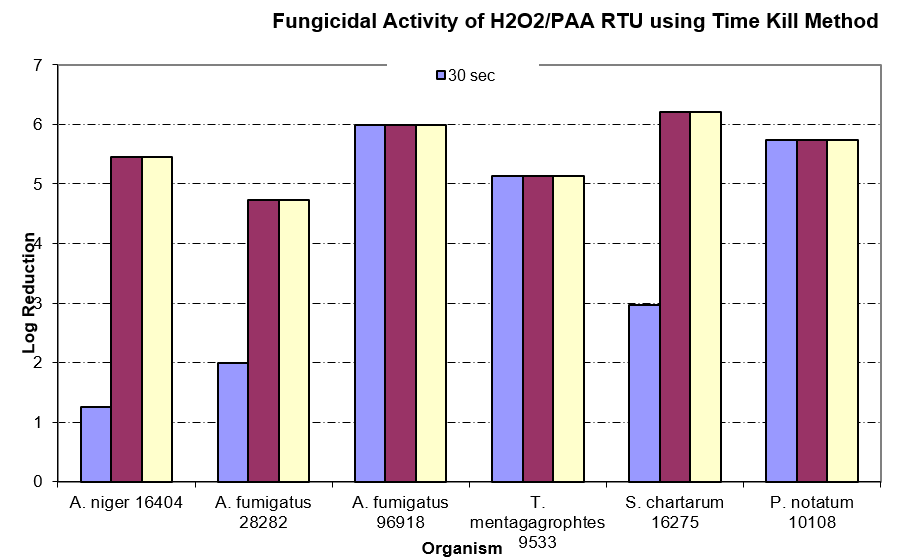
L'alcol è un altro agente utilizzato nelle camere bianche che non sempre viene utilizzato correttamente. Molte strutture utilizzano solo alcol isopropilico (IPA) al 70% sugli oggetti che saranno trasferiti nell'ambiente della camera bianca, dando per scontato che sia efficace contro le spore fungine e batteriche. È possibile che abbia qualche effetto sulle spore fungine, come dimostra la tabella sottostante (studio time-kill2), ma occorre uno sporicida vero e proprio per impedire l'ingresso di microrganismi sporigeni nella camera bianca
Efficacia di H2O2/PAA pronto all'uso (RTU) contro le muffe
Spesso gli operatori sono addestrati, secondo le SOP, a utilizzare movimenti sovrapposti unidirezionali con spazzoloni a testa piatta su pareti e pavimenti… Tuttavia, questa tecnica può peggiorare la situazione, se gli operatori non sono adeguatamente formati e le procedure non vengono applicate rigorosamente. Un altro elemento fondamentale per una disinfezione efficace è rappresentato dalla corretta diluizione del prodotto3. Cilindri graduati e bustine monodose rappresentano il metodo più preciso. Non è mai consigliabile versare il disinfettante concentrato in un secchio usando il metodo "a occhio".
Un programma di pulizia e disinfezione efficace deve sempre includere un disinfettante ad ampio spettro di efficacia e uno sporicida per contrastare le endospore batteriche nelle operazioni che si svolgono nelle camere bianche.

(Image Credit: http://www.pppmag.com/article/714/June_2010/Cleaning_Practices_for_Cleanroom_Contamination_Control/)
Mito: i residui di disinfettante possono accumulare carica batterica e compromettere l'efficacia di uno sporicida
Per mantenere il controllo ambientale delle camere bianche è necessaria l'applicazione periodica di agenti disinfettanti e sporicidi. L'uso periodico di questi prodotti può lasciare residui sulla superficie. La rotazione di prodotti chimici incompatibili può causare problemi, ma i residui di disinfettante da soli favoriscono la contaminazione microbica? Inoltre, i residui di disinfettante interferiscono con l'efficacia sporicida?
I disinfettanti fenolici di ultima generazione di STERIS sono stati testati sotto forma di residui in uno studio time-kill volto a valutare l'impatto sull'efficacia di uno sporicida (SporKlenz® RTU) rispetto a Bacillus subtilis, ATCC n. 19659. I solidi (µg/cm2) derivanti dai residui di disinfettante essiccato sono stati misurati in uno studio separato, in cui la quantità di residuo è stata calcolata dopo diverse applicazioni su un provino di acciaio inossidabile da 116 cm2 per simulare l’uso tipico nelle camere bianche, così come la quantità di SporKlenz RTU necessaria per coprire una superficie nelle applicazioni abituali come diluente. In quest’ultimo caso si è accertato che 120 mg di SporKlenz RTU sterilizzante sono necessari per coprire un provino da 116 cm2. I rapporti determinati in quest’esperimento sono stati estrapolati per stabilire la diluizione del residuo disinfettante da aggiungere a una soluzione di sporicida.
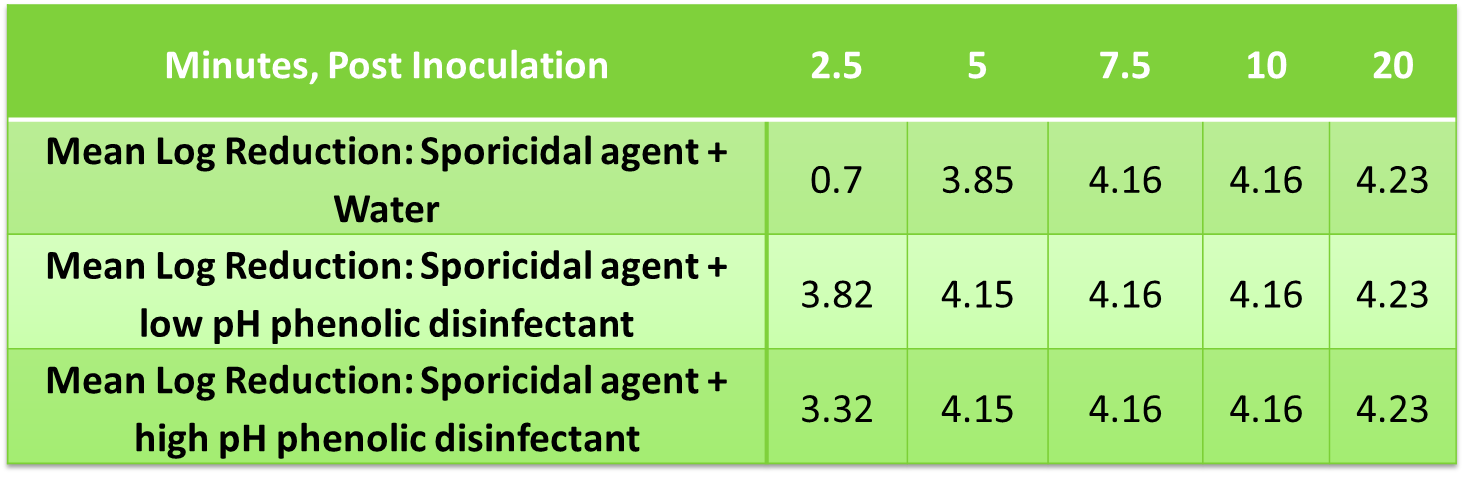
Un volume di 0,1 mL della sospensione di microrganismi è stato aggiunto a 9,9 mL della soluzione di prova (vale a dire, sterilizzante Spor-Klenz RTU arricchito con un disinfettante fenolico a pH basso o alto). La stessa quantità è stata inoculata in un tampone di controllo. Dopo l'inoculazione, è stato prelevato un campione di 0,1 mL a 2,5, 5, 7,5, 10 e 20 minuti. I campioni sono stati neutralizzati, seminati su piastra e incubati per 48-49 ore a 37 ± 2 °C. Gli organismi vitali per mL di campione sono stati stabiliti sulla base di una conta standard su piastra aerobica.
Riduzione logaritmica media di B. subtilis utilizzando residui fenolici e soluzione di sporicida
Allo stesso modo, sono stati valutati i residui di disinfettante essiccato per stabilire l'impatto sull'efficacia sporicida, poiché ciò riflette le pratiche generalmente utilizzate nelle camere bianche. I campioni sono stati preparati in modo da rappresentare 20 giorni di applicazione di disinfettante su un'area nota, lasciati asciugare, quindi trattati con un volume di sporicida sufficiente a coprire l'area nota o 8,6 µL/cm2. L'inoculo è stato preparato da una sospensione di spore di Bacillus subtilis, numero ATCC 19659. La sospensione di spore è stata diluita con acqua deionizzata fino a circa 3,0 x 108 CFU/mL. La sospensione è stata aggiunta a provette contenenti campioni di prova o tampone Butterfields per ottenere una miscela all'1% v/v di microrganismi nel prodotto di prova o nel tampone. In vari momenti, i campioni sono stati neutralizzati, seminati su piastra e incubati per 48 - 50 ore a 37 ± 2 °C dopo l'inoculo. Gli organismi vitali per mL di campione sono stati stabiliti sulla base di una conta standard su piastra aerobica e convertiti in valori logaritmici decimali per l'analisi.
Riduzione logaritmica media di B. subtilis utilizzando residui fenolici essiccati e soluzione di sporicida
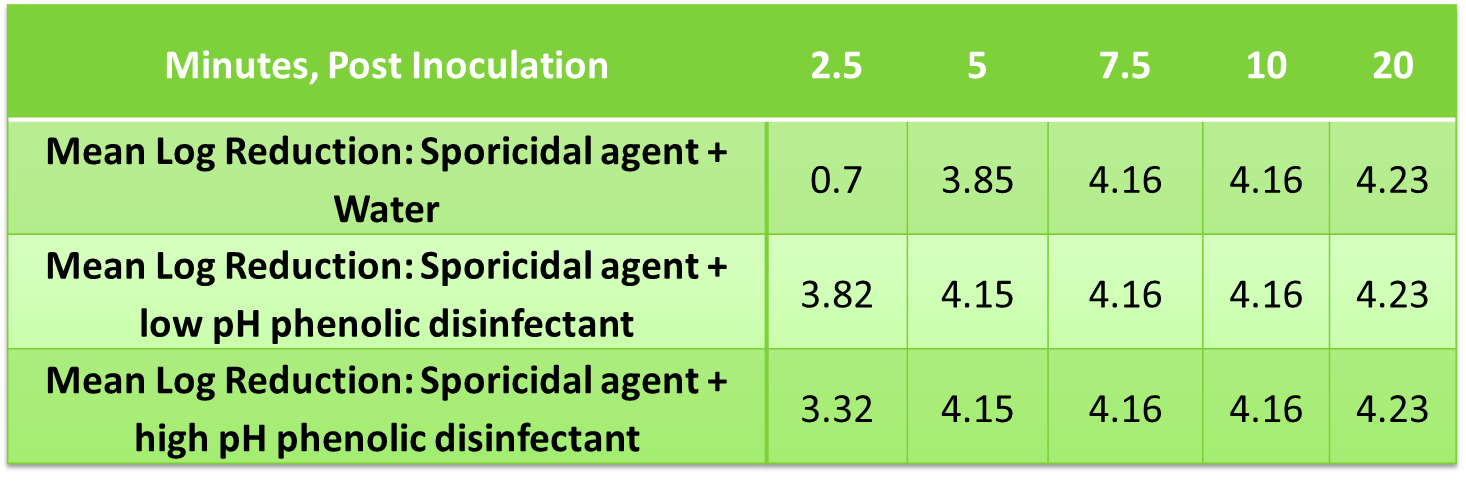
I dati non evidenziano effetti inibitori/antagonisti del residuo essiccato con efficacia sporicida.
Formazione di base
È deplorevole che nelle aziende produttrici di biofarmaceutici, formulazioni solide orali (OSD) e dispositivi medici le “squadre di pulizia”, che si occupano della sanificazione con disinfettanti nelle aree di produzione con camere bianche regolamentate, ricevano spesso meno formazione, indicazioni e supervisione rispetto ad altri reparti (ad esempio QC, Produzione). Spesso, nell'ottica di risparmiare sui costi, il ruolo della pulizia tramite disinfettanti viene affidato a un'impresa di pulizie a contratto, complicando ulteriormente le questioni relative alla formazione ed esonerando il personale addetto alle pulizie dalla supervisione da parte dei reparti QC e QA. Le ore di straordinario rendono ancora più difficile comprendere che cosa accade in produzione. Nell'attuale mercato globale, anche le barriere linguistiche possono costituire un problema. A complicare ulteriormente le cose, la disinfezione efficace delle superfici e degli ambienti delle camere bianche dipende interamente dalle capacità e dalla tecnica dell'operatore. A differenza della pulizia fisica dello sporco visibile, le superfici delle camere bianche di solito appaiono già pulite. I dipendenti hanno quindi il compito di rimuovere lo sporco invisibile, che sia una carica biologica vitale o una contaminazione da particolato sub-visibile. Gli indizi visivi indicativi dell’avvenuta decontaminazione di una superficie sono pochi o assenti. Per queste ragioni, gli operatori addetti alla pulizia con disinfettanti devono essere eccezionalmente ben formati e preparati sui principi di microbiologia, controllo della contaminazione e pratiche asettiche.
Bibliografia:
- PDA Technical Report No. 70 (2015). Fundamentals of Cleaning and Disinfection Programs for Aseptic Manufacturing Facilities. Available from Parenteral Drug Association, Inc.
- Polarine, J., Macauley, J., Karanja, P., Klein, D., Martin, A. (2009) Evaluating the Activity of Disinfectants Against Fungi. Cleanrooms: The Magazine of Contamination Control Technology 23(2).
- http://www.pppmag.com/article/714/June_2010/Cleaning_Practices_for_Cleanroom_Contamination_Control/
Contenuti consigliati
Un processo giustificato per la pulizia e la disinfezione
Best practice per la convalida dei disinfettanti nelle camere bianche
Rimozione dei residui nelle camere bianche: una panoramica normativa
Iscriviti alla nostra mailing list per ricevere le ultime novità del settore e gli aggiornamenti sui prodotti.
Cliccando su Iscrizione confermi di accettare i nostri Termini e condizioni.



